生物标志物
- 悬浮科技赋能生物标志物发现
生物标志物(Biomarker)的基本定义是指作为正常生物学过程、发病过程、外界暴露或干预反应的一个可测量指标 1。基于用途可细分为诊断性、监测性、药效学/反应性、预测性、预后性、安全性和易感性/风险性等生物标记物亚类 2。近年来在精准医学领域展现出巨大潜力。
随着纳米、人工智能、单细胞多组学分析等技术的突破,生物标志物的发现与应用进入新的阶段,逐渐成为疾病诊断、治疗监测及预后评估的关键工具之一。例如,肿瘤精准治疗方面,肿瘤浸润淋巴细胞(TIL)作为肿瘤免疫疗法的治疗生物标记物 3、外周血中TRGC2+ NKT细胞增殖与辅助治疗效果高度关联 4;在慢性病管理方面,:应用T细胞受体作为1型糖尿病发病过程的生物标记物 5,卒中(俗称“中风”)后的精准医学治疗干预 6。
生物标志物开发与应用过程中的“绊脚石”
尽管生物标志物的研究取得了显著进展,但其在标志物开发、标准化验证及临床转化等方面仍面临诸多挑战。然而,传统的生物标志物鉴定方法由于肿瘤异质性及肿瘤微环境的复杂性,往往面临着巨大的挑战。随着新技术的不断推出与应用,为这一领域提供了新的机遇。诸如单细胞测序技术(sc-Seq)可以深入分析肿瘤组织中的细胞组成,不仅能够识别不同的细胞亚群以构建肿瘤的单细胞图谱,还能够了解这些细胞在肿瘤进程中的功能及其相互作用,从而对细胞间的差异进行基因和通路层面的深入研究,为生物标志物的开发提供了一种全新的思路。7, 8 而单细胞多组学分析等技术起步的第一块绊脚石便是细胞样本制备,须考量:
细胞异质性与样本代表性的保留
肿瘤组织或肿瘤微环境由多种细胞种类及同种细胞类型的多种亚型组成,这些不同细胞类型的精确比例与疾病进程息息相关 4。若要通过检测特定细胞种类或亚型来作为生物标志物,则需确保检测(如单细胞测序)前细胞样本制备过程中各类细胞的完整保留。否则,会造成下游检测结果的误差,如肺癌微环境中的免疫抑制性T细胞可能因采样偏差被遗漏9。
高细胞活性与完整性
细胞类样本的制备需要最大化保障回收细胞的完整性与活性,以避免生物标志物的降解或丢失,如常规解离过程可破坏细胞骨架结构,进而影响细胞力学特性测量结果的准确性 10;此外,若下游应用单细胞测序等技术检测,则须满足高细胞活性要求(通常不低于70%)11。

利用悬浮技术揭示疾病背后隐藏的生物学特征
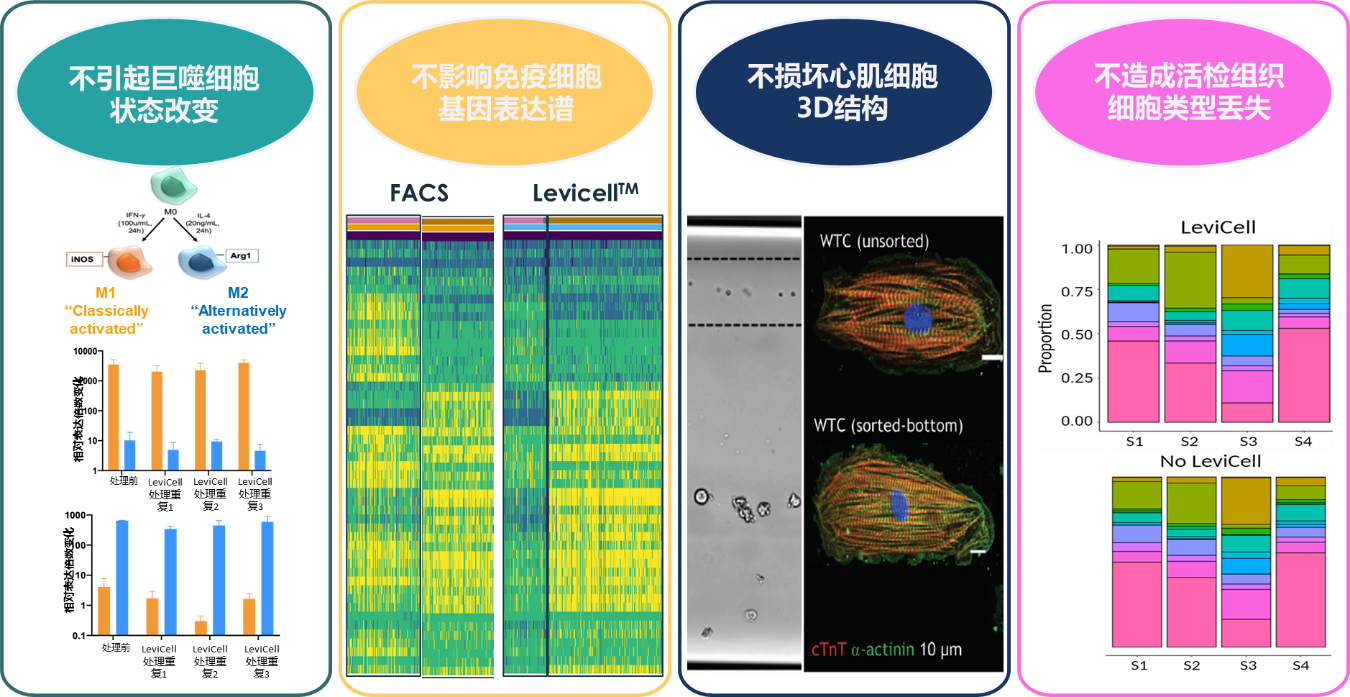
是否有办法让人确信所获得的数据真实反映了生物样本的客观特征?传统的单细胞制备方法往往会损伤细胞,降低细胞活力。在减少可用于下游研究的细胞数量的同时,更重要的是多重操作的压力与流程可改变细胞状态、基因表达谱特征或所研究细胞群的生物学特征。
悬浮技术(Levitation Technology™)能从碎片、死细胞和其他细胞类型中分离并富集高活力的细胞,同时将操作时间和处理步骤减少80%以上。利用LeviCell®系统简便的3步操作方案,即使是最脆弱、最敏感的细胞也能被高效的富集回收。其快速、轻柔的特性,还可最大化保留细胞原生状态,且全程无需额外染色或标记,保证了不偏不倚的回收所有类型的活细胞。
- FDA-NIH Biomarker Working Group. BEST (Biomarkers, EndpointS, and other Tools) Resource. Silver Spring (MD): Food and Drug Administration (US); Bethesda (MD): National Institutes of Health (US), ncbi.nlm.nih.gov/books/NBK326791/.
- Califf RM. Biomarker definitions and their applications. Exp Biol Med (Maywood). 2018 Feb;243(3):213-221.
- Lopez de Rodas M, Villalba-Esparza M, Sanmamed MF, et al. Biological and clinical significance of tumour-infiltrating lymphocytes in the era of immunotherapy: a multidimensional approach. Nat Rev Clin Oncol. 2025 Mar;22(3):163-181.
- Shang X, Xie Y, Yu J, et al. A prospective study of neoadjuvant pembrolizumab plus chemotherapy for resectable esophageal squamous cell carcinoma: The Keystone-001 trial. Cancer Cell. 2024 Oct 14;42(10):1747-1763.e7.
- Nakayama M, Michels AW. Using the T Cell Receptor as a Biomarker in Type 1 Diabetes. Front Immunol. 2021 Nov 17;12:777788.
- Simpkins AN, Janowski M, Oz HS, et al. Biomarker Application for Precision Medicine in Stroke. Transl Stroke Res. 2020 Aug;11(4):615-627.
- Bai Z, Su G, Fan R. Single-cell Analysis Technologies for Immuno-oncology Research: from Mechanistic Delineation to Biomarker Discovery. Genomics Proteomics Bioinformatics. 2021 Apr;19(2):191-207.
- Radpour R, Forouharkhou F. Single-cell analysis of tumors: Creating new value for molecular biomarker discovery of cancer stem cells and tumor-infiltrating immune cells. World J Stem Cells. 2018 Nov 26;10(11):160-171.
- Nooreldeen R, Bach H. Current and Future Development in Lung Cancer Diagnosis. Int J Mol Sci. 2021 Aug 12;22(16):8661.
- Eroles M, Rico F. Advances in mechanical biomarkers. J Mol Recognit. 2023 Aug;36(8):e3022.
- Tastanova A, Ramelyte E, Balázs Z, et al. Collection and preprocessing of fine needle aspirate patient samples for single cell profiling and data analysis. STAR Protoc. 2021 Jun 5;2(2):100581.