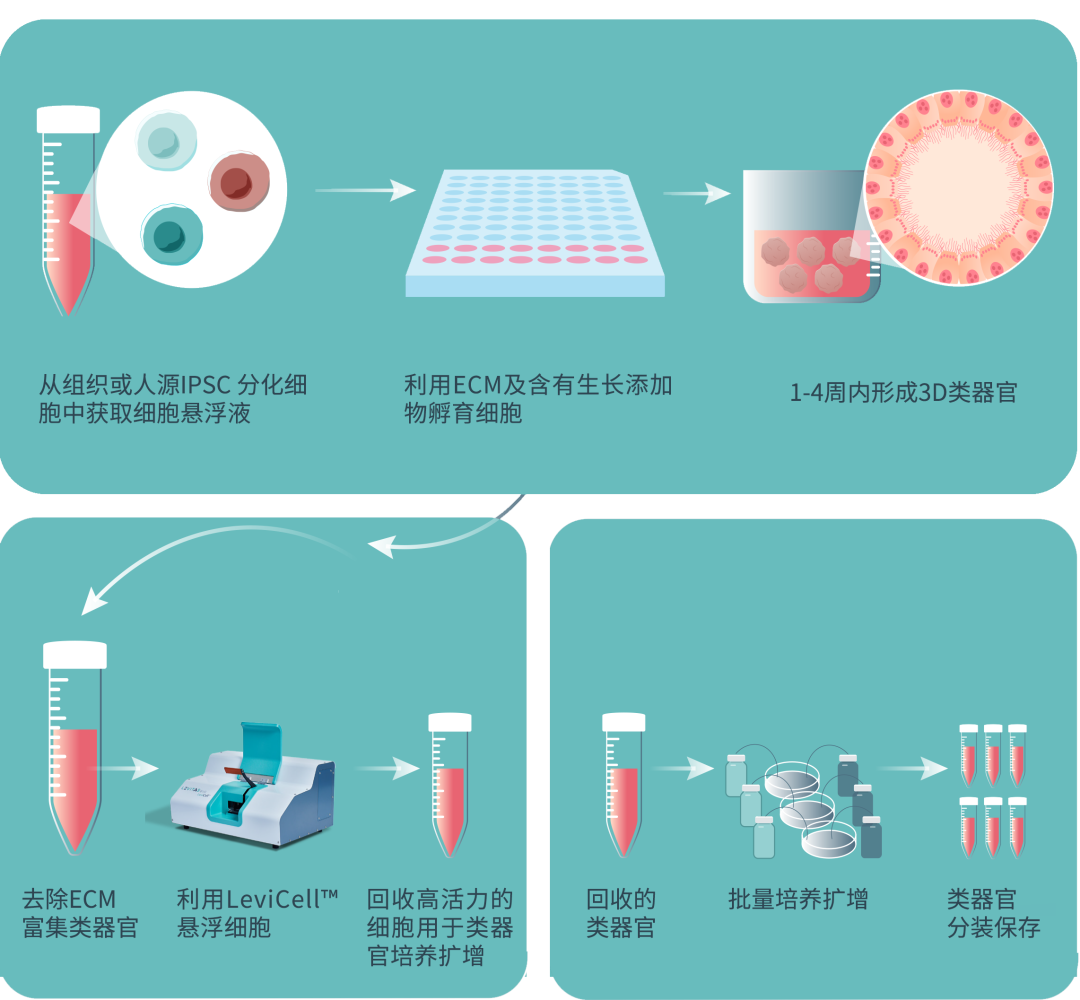
类器官
LeviCell®的创新性、无标记分离技术可彻底去除碎片和死细胞,而不会影响基因表达的原始种群(请参阅《细胞群表征》章节说明,以了解有关LeviCell®如何保持原始种群特征的额外数据)。对于单细胞研究,从样品制备阶段中收获的细胞的纯度和活力是在诸如NGS(下一代测序)之类的下游分析中生成高质量数据的决定性因素。LeviCell®可无缝地富集目标细胞并产生稳定的活细胞产量,而无需优先消耗或改变细胞类型的频率或表达,使其具有许多科学家一直在等待的必要技术特征,以将它们带入一个新的高度。
类器官如何改变转化医学研究
生物学家通过动物模型、二维细胞培养和三维有机体来研究细胞过程。模型生物和二维细胞培养技术都具有独特的优势,但它们无法捕捉复杂的人体生理和疾病机理
机制。而类器官在结构和功能上可模拟体内组织,是最精确的模型系统之一。
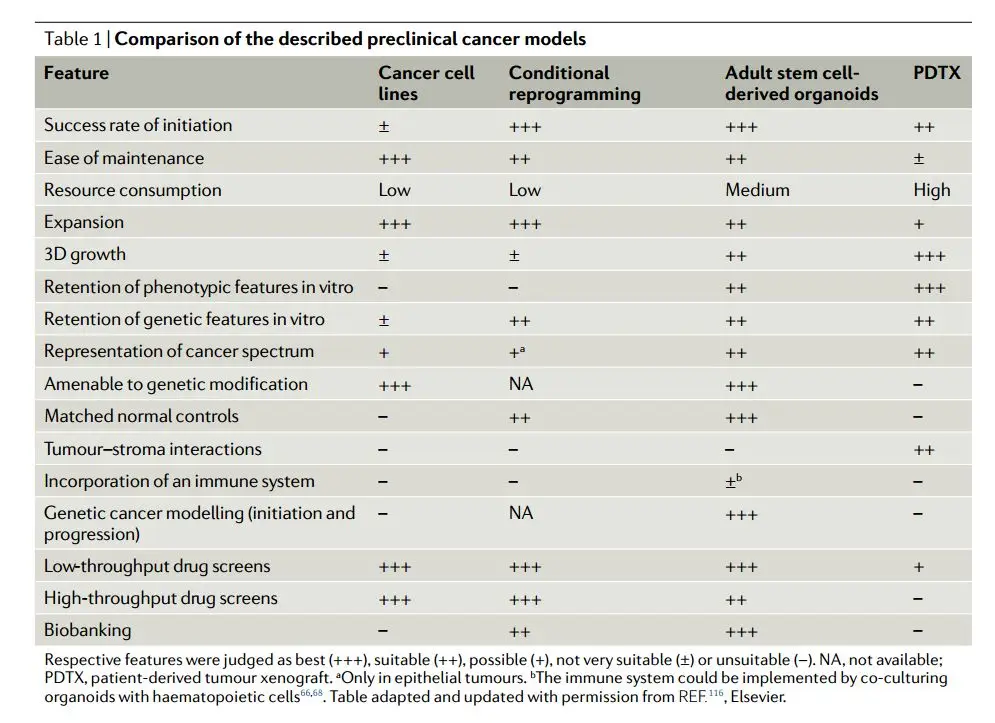
临床前癌症模型的比较(Drost J et al., 2018)
应用前景
类器官在发育生物学、疾病建模、再生医学、药物筛选、癌症研究等领域有着巨大的应用前景:
个性化精准诊疗
患者来源的肿瘤类器官(Patient-Derived Tumor Organoids, PDOs)保留了原发肿瘤的遗传特征,可用于个性化药物筛选及治疗方案优化。有研究显示,类器官药敏测试的临床预测准确率可达88%(阳性率)和100%(阴性率)。
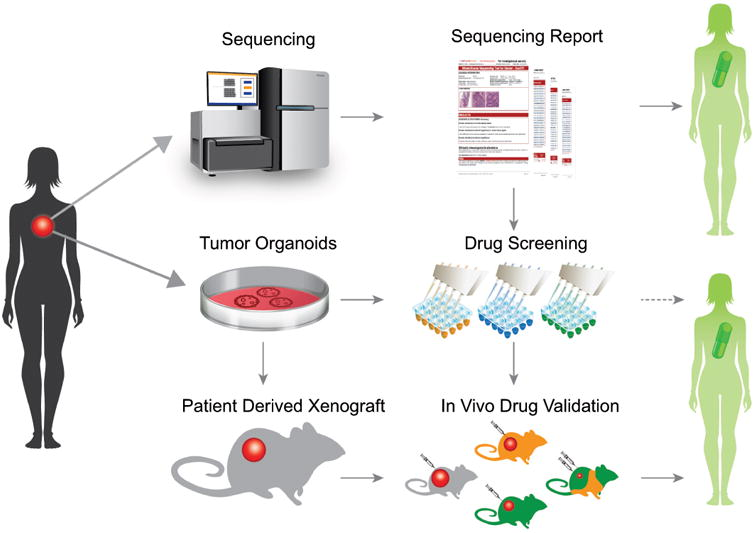
指导晚期癌症个性化精准医疗的模型(Drost J et al., 2018)
理想的器官或疾病模型
类器官通过自组织形成三维结构,能够高度模拟体内器官的复杂空间排列与功能,其细胞间相互作用、细胞-基质信号传递更接近真实生理环境,适用于研究器官发育、疾病激励机制等研究,如已建立的人肠类器官 、人脑类器官 、人乳腺癌类器官 、人前列腺癌类器官等。
类器官培养以及扩增时面临的问题
当前,类器官的培育仍存在一些问题。从将单个细胞或组织片段悬浮在支持性结构(如ECM)中,让它们在含有生长因子、小分子、重组蛋白及其他添加物的培养基中生长为类器官。为增加下游实验所需数量,需对类器官进行亚培养或传代,即通过溶解与离心去除原ECM,收获类器官,再使用酶或机械方法解离类器官后,将其悬浮在新ECM 中,以增殖更多类器官。成功的扩增过程可保持类器官复杂的组织结构、特化功能和疾病表型,因而要求获得具有高活力和均质的类器官系,其组成细胞类型比例精确,批次间差异最小。然而,培养类器官需要许多复杂的准备步骤与注意事项,这些都可能直接的负面影响:
- 在细胞扩增的每个环节中都保持细胞高活力及细胞类型的精确比例仍是一项挑战;
- 在每一个传代步骤中,培养物都会带入非增殖的死细胞与碎片,从而减慢细胞生长速度。随着时间的推移,生长缓慢和缺乏活力的培养物在多次传代后便不再增殖,可导致类器官系的消失;
- 商业售卖的冷冻保存的类器官是很好的起始材料,但冻融循环和储存时间会进一步降低类器官系的细胞健康、恢复和均匀性。
LeviCell®悬浮细胞、优化流程
LeviCell®系统基于创新的 Levitation Technology™(磁悬浮技术),可为下游应用富集高质量的细胞或类器官。当细胞或类器官被引流到系统内置磁场中后,高活力的细胞或类器官将悬浮于芯片的上方,而死细胞及碎片则会悬浮于芯片的下方,从而通过悬浮高度的差异来分离富集高活力细胞或类器官。在利用类器官来源的单细胞悬液进行CRISPR工作流程的研究人员也将受益于LeviCell®系统。可于转染前后富集活细胞提高转染效率,以增加转染类器官的产量,并缩短周转时间,因为下游培养中将不存在死细胞及碎片。

类器官培养以及批量扩增的工作流程
自这项技术问世以来,研究人员主要通过人工方法培育类器官。待培育完成后,可通过移除ECM、酶解和/或机械解离细胞,利用LeviCell®系统快速、轻柔、无标记的富集高活力细胞,以确保高质量的单细胞产量,最终进行传代培养,扩增更多的类器官数量。考虑到扩增培育过程耗时、耗力,而且需要技术熟练的人员,同时降低样本丢失风险与批次间的可变性,可采用成熟的批量生物处理技术进行类器官的规模生产。